- 作者: Kilby-Biot
- 来源:
- 日期 : 2026-05-06

一、研究概述与背景
1.1 行业痛点
药物诱导的QT间期延长和尖端扭转型室性心动过速(Torsades de Pointes, TdP)是药物研发失败和撤市的主要原因之一。现行临床前评价策略存在明显局限:
hERG单一通道检测:特异性差,导致大量有前景的候选药物被过早淘汰;
动物实验:种属差异大,且处于临床前后期,错失了早期分子优化窗口;
传统2D培养:细胞呈异步搏动,无法真实模拟3D心肌微环境,功能成熟度低。
1.2 BiomimX的解决方案
BiomimX Srl(意大利米兰)开发了一种名为 uHeart 的3D人体心脏器官芯片(heart-on-chip)模型,并配套 uBeat 平台与 mECG(微电极通道引导) 电生理记录技术。
本研究旨在通过一项包含11种已知临床风险等级药物的药理学 campaign,系统验证 uHeart 作为符合 ICH S7B/E14 指南的临床前心脏安全性筛选工具的可靠性。
BiomimX器官芯片中国区授权销售——北京基尔比生物公司【详情请查阅-官网】
二、BiomimX uHeart 平台技术详解
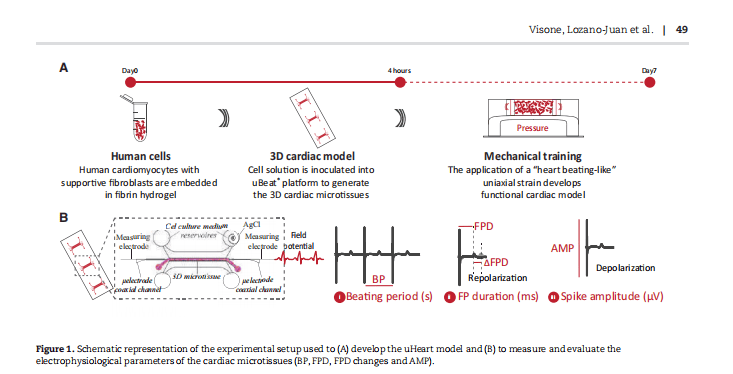
2.1 3D心脏微组织构建流程
- 细胞配比:75% 人诱导多能干细胞来源心肌细胞(h-iPSC-CMs,FUJIFILM Cellular Dynamics)+ 25% 人皮肤成纤维细胞(Lonza);
- 水凝胶包埋:细胞密度 125×10⁶ cells/mL,嵌入纤维蛋白水凝胶(10 mg/mL 纤维蛋白原 + 1.25 U/mL 凝血酶);
- 芯片接种:将2 µL细胞悬液注入 uBeat 平台中央通道,37°C交联8分钟;
- 机械训练:接种后4小时开始施加 10% 单轴应变、1 Hz 的"类心跳"机械刺激,持续7天;
- 功能成熟:培养至第6-7天,微组织形成自发同步搏动,即可进行电生理检测。
2.2 技术突破点
- 3D+力学耦合:相比传统2D MEA培养,uHeart 通过3D空间结构和机械训练,在 7天内 即可形成功能性合胞体搏动,而传统2D模型通常需要10-14天以上;
- 全局场电位:由于组织同步搏动,uHeart 记录到的是代表整个微组织的全局FP信号,无需像2D MEA那样从多个异步信号中筛选"金标准"信号;
- 在线监测:mECG技术实现了对3D搏动心脏微组织的在线、连续电生理监测。
三、研究方法与实验设计
3.1 药物选择
研究严格遵循 CiPA(Comprehensive in Vitro Proarrhythmia Assay) 倡议和 ICH S7B 指南,选取11种化合物:
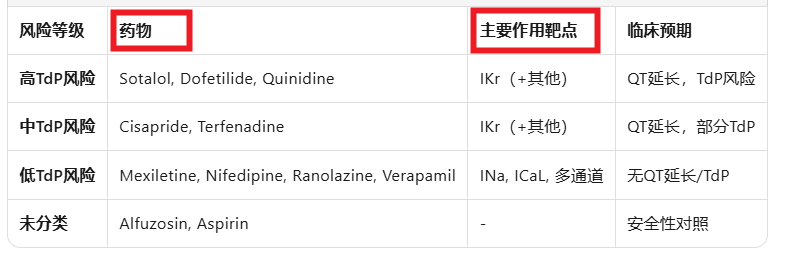
3.2 给药与检测协议
- 基线记录:无血清RPMI培养基平衡1小时后,记录至少3分钟基线FP;
- 递增剂量:从最低浓度开始给药,孵育10-20分钟后记录FP,每次增量前用无血清RPMI洗涤5分钟;
- 评价参数:搏动周期(BP)、场电位时程(FPD)、Fridericia校正FPD(FPDcF)、 spike振幅(AMP)、心律失常事件、自发搏动停止。
3.3 质控标准
- 纳入标准:基线BP的变异系数(CV)< 25%;
- 60个微组织中51个符合标准(合格率85%),平均CV约13%。

四、核心研究结果
4.1 对校准化合物的响应(单通道阻断剂)
Dofetilide(IKr阻断):浓度依赖性FPDcF延长,高剂量导致1/3样本停搏;
Nifedipine(ICaL阻断):浓度依赖性FPDcF缩短;
Mexiletine(INa阻断):对FPDcF无明显影响,但浓度依赖性降低AMP。
结果与临床预期及FDA标签高度一致。
4.2 对测试化合物的响应(多通道/临床风险药物)
高TdP风险药物:Sotalol、Dofetilide、Quinidine、Terfenadine 均引起FPDcF显著延长,且 Dofetilide、Quinidine、Terfenadine 诱发心律失常;
中TdP风险药物:Cisapride 未延长FPDcF(反而缩短),但诱发心律失常并导致停搏;Terfenadine 成功被识别(而此前2D MEA研究曾将其误判为假阴性);
低TdP风险/阴性药物:Nifedipine、Verapamil 缩短FPDcF;Mexiletine、Aspirin 对FPDcF无显著影响;
Ranolazine:虽为低TdP风险,但在uHeart中表现出FPDcF延长和心律失常(与部分2D研究一致,但临床标签未报告TdP,属于假阳性)。
五、BiomimX公司uHeart 器官芯片平台性能验证
研究以 FDA药物标签 为金标准,评估了uHeart预测QT延长和TdP风险的性能:
5.1 QT/QTc延长预测(以MID阈值15%为cut-off)

5.2 TdP风险/心律失常预测

5.3 与2D MEA系统的对比
尽管测试化合物数量(11种)少于CiPA研究(28种),uHeart在检测FPD变化方面:
特异性:100%(与2D iCell/MEA持平)
灵敏度:83.3%(优于2D的80%)
准确率:91.6%(优于2D的86%)
在心律失常检测方面,BiomimX公司uHeart(灵敏度80%,特异性85.7%)显著优于2D MEA系统(灵敏度50%,特异性66%)。
六、BiomimX 平台的商业化与科学意义
6.1 作为临床前工具的优势
- 人源化:完全基于人iPSC-CMs,避免动物种属差异;
- 快速:7天内形成功能性同步搏动微组织,实验周期短于动物模型(2-4周);
- 符合监管指南:实验设计遵循ICH S7B/E14最佳实践,FPD校正采用Fridericia法;
- 成本可控:所需细胞数量与标准48孔板2D培养相当,属于中等通量范围;
- 多参数读出:同时提供QT延长、心律失常、搏动停止、振幅变化等多维度安全性指标。
6.2 局限性与未来方向(BiomimX技术迭代空间)
细胞成熟度:iPSC-CMs仍呈胎儿样表型,未来可通过延长培养时间或替换为心脏成纤维细胞进一步提升电生理成熟度;
代谢缺失:当前模型缺乏药物代谢酶(如CYP450),可能影响前体药物(如Terfenadine)的评估,未来可整合肝芯片或代谢酶系统;
给药方案:本研究采用递增剂量方案,可能因累积毒性干扰高剂量数据,未来可引入单剂量实验设计;
算法升级:当前软件已实现75%的数据分析时间缩减,未来将进一步开发心律失常事件的自动分类功能。
七、作者与利益相关声明
- BiomimX Srl 为本文核心技术的商业载体,地址位于意大利米兰(20158)。
- 研究获得欧盟 Horizon 2020 研究与创新计划(Marie Skłodowska-Curie 资助协议)支持。
总结
本文系统验证了 BiomimX 公司开发的 uHeart 3D心脏芯片平台 在临床前心脏安全性评价中的可靠性。通过将人iPSC-CMs与成纤维细胞在纤维蛋白水凝胶中3D培养,并结合 uBeat 平台的机械训练与 mECG 在线电生理记录技术,uHeart 能够在7天内形成功能性同步搏动的心脏微组织。
对11种CiPA参考药物的评价显示,该平台以 83.3%的灵敏度、100%的特异性和91.6%的准确率 成功预测了药物诱导的QT延长,并在心律失常检测方面显著优于传统2D MEA系统。
BiomimX 公司开发的 uHeart 符合ICH S7B指南要求,是一种具有高度转化医学价值的临床前心脏安全性筛选工具,有望补充甚至替代部分动物实验和2D hERG筛选,加速药物研发进程并降低后期临床失败风险。
![]()

